HS-GC/MS/MSによる天然ゴム中オフフレーバー分析 [GC-TQMS Application]
MSTips No. 406
はじめに
天然ゴムは、靴底やホースなどの日用品から、タイヤなどの工業製品まで幅広く使用されている。一方、天然ゴムの木の樹液は匂いが強いため、天然ゴムに含まれるオフフレーバー成分の管理が重要となる。一般的な分析方法としては、HS-GC/MSによるSCAN/SIM測定が用いられる。しかし、天然ゴムによっては夾雑成分が多く含まれているため、SIM測定では夾雑成分の影響を受けてしまう可能性がある。そのため、SIM測定では微量に含まれるオフフレーバー成分の分析が困難となる。これに対し、GC/MS/MSのSRM測定であれば、選択したプリカーサーイオンとプロダクトイオンの組み合わせによる測定となるため、夾雑成分からの影響を抑えることができると共に、SIM測定よりも多くのイオンを用いた測定となるため、微量成分の定性解析能力も向上する。さらに、JEOLのHSのケミカルトラップモードとSRM測定を併用することで、より高感度な測定が可能となり、測定に用いる試料量を減らすことができる。今回は、HS-GC/MS/MSを用いて、天然ゴムに含まれるオフフレーバー成分を分析したので報告する。
測定条件
測定はトラップ型ヘッドスペース装置 MS-62071STRAP と、ガスクロマトグラフ三連四重極質量分析計JMS-TQ4000GC UltraQuad™ TQを使用した。測定試料として、天然ゴム(サンプルAとサンプルB)を用いた。サンプルAはオフフレーバー成分が多く、サンプルBは少ない試料となっている。試料量は通常200 mg使用するところを50 mgに減らして測定を実施した。Table 1に測定条件を示し、Table 2に測定対象成分とそのSRMトランジションを示す。
Table 1 Measurement condition
| HS condition | |
|---|---|
| Sample Temp. | 150°C |
| Sampling mode | Trap mode |
| Heating time | 20 min |
| Trap tube | AQUATRAP1 (GL Sciences Inc.) |
| GC condition | |
| Column | VF-5MS(30 m length, 0.25 mm i.d., 0.25 μm film thickness) |
| Inlet | Split/Splitless |
| Inlet Temp. | 250°C |
| Flow | 2 mL/min, Constant flow |
| Injection Mode | Split (20 :1) |
| Oven Program | 40 °C (3 min) → 3 °C/min → 100 °C (1min) → 8 °C/min → 250 °C |
| MS condition | |
| Ion Source Temp. | 200 °C |
| Interface Temp. | 250 °C |
| Ionization Mode | EI+, 70 eV |
| Measurement Mode | SCAN, SRM |
| Mass range | m/z 10-500 |
| Collision Gas | N2, 10% |
Table 2 SRM transition
| Compound | R.T.(min) | Quantitative ion | Reference ion 1 | Reference ion 2 |
|---|---|---|---|---|
| Acetic acid | 1.7 | 60->43 CE:5 | 60->45 CE:10 | 60->60 CE:5 |
| Isovaleric aldehyde | 2.1 | 44->43 CE:15 | 58->57 CE:10 | 58->58 CE:5 |
| Propionic acid | 2.6 | 74->55 CE:15 | 74->73 CE:15 | 57->57 CE:5 |
| Isobutyric acid | 3.6 | 73->55 CE:10 | 88->73 CE:15 | 73->73 CE:5 |
| Toluene | 3.7 | 91->65 CE:15 | 92->91 CE:15 | 92->92 CE:5 |
| Butyric acid | 4.5 | 60->42 CE:10 | 73->55 CE:10 | 60->60 CE:5 |
| Isovaleric acid | 6.2 | 60->42 CE:15 | 87->69 CE:10 | 60->60 CE:5 |
| Valeric acid | 7.9 | 60->42 CE:10 | 73->55 CE:10 | 60->60 CE:5 |
| Skatole | 28.6 | 130->77 CE:20 | 130->130 CE:10 | 131->130 CE:15 |
結果
サンプルAとサンプルBのSCAN測定結果
Fig.1にサンプルAのTICCとEICを示す。サンプルAはオフフレーバー成分を多く含んでいるため、SCAN測定において明確に目的成分のクロマトグラムピークが確認された。同様にして、サンプルBもピーク強度は弱いものの同じRTにクロマトグラムピークが確認された。
| No. | Compound |
|---|---|
| 1 | Acetic acid |
| 2 | Isovaleric aldehyde |
| 3 | Propionic acid |
| 4 | Isobutyric acid |
| 5 | Toluene |
| 6 | Butyric acid |
| 7 | Isovaleric acid |
| 8 | Valeric acid |
| 9 | Skatole |
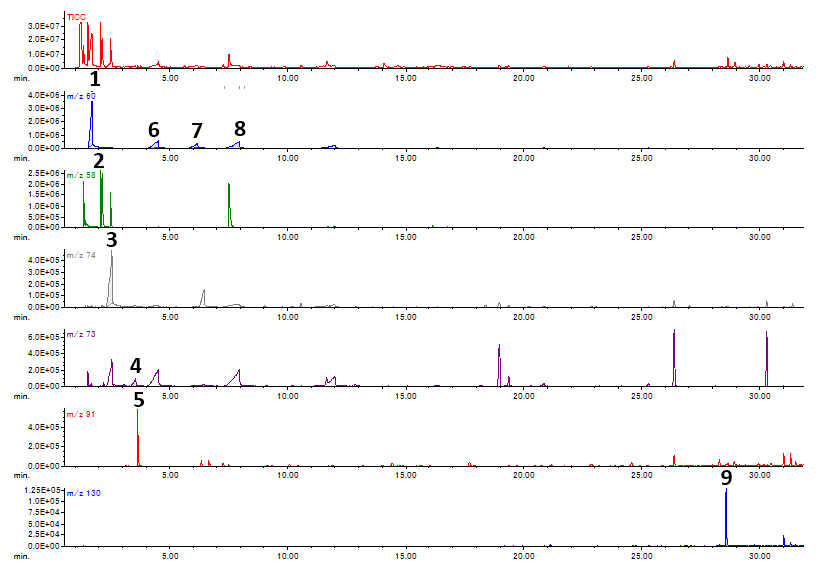
Fig. 1 TICC and EIC of Sample A
サンプルAとサンプルBのNISTライブラリーサーチ結果
Table 3にNISTライブラリーサーチ結果におけるM.F.の値を示し、Fig. 2にValeric acidとSkatoleのマススペクトルを示す。サンプルAはオフフレーバー成分の含有量が多いため、820~938と高いM.F.の値が得られた。サンプルBはオフフレーバー成分の含有量が少ないため、NISTライブラリーサーチ結果では、半数以上でM.F.の値が低い、もしくは目的成分の検索結果を得られなかった。Fig. 2に示すように、サンプルBから得られたValeric acidとSkatoleのマススペクトルはサンプルA及びNISTライブラリーデータとは大きく異なっていた。サンプルBから観測されたクロマトグラムピークは主に夾雑成分により構成されていることがわかる。このため、SIM測定を行った際には、夾雑成分の影響を大きく受けてしまうことが予想されるため、夾雑成分の影響を抑えることができるSRM測定が適した測定方法となる。
Table 3 NIST library search result
| No. | Compound | M.F. | |
|---|---|---|---|
| Sample A | Sample B | ||
| 1 | Acetic acid | 932 | 892 |
| 2 | Isovaleric aldehyde | 932 | 933 |
| 3 | Propionic acid | 845 | 731 |
| 4 | Isobutyric acid | 868 | 725 |
| 5 | Toluene | 938 | 940 |
| 6 | Butyric acid | 822 | 618 |
| 7 | Isovaleric acid | 900 | 853 |
| 8 | Valeric acid | 859 | - |
| 9 | Skatole | 820 | - |
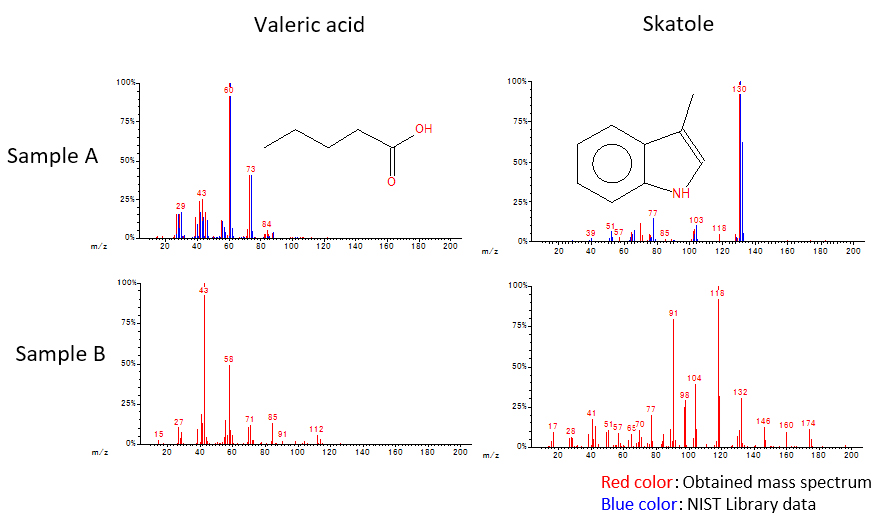
Fig. 2 The difference of mass spectra by influence of contaminant
サンプルBの各成分におけるピーク面積値の再現性
Table 4にSCAN測定により得られたピーク面積値の再現性を示し、Table 5にSRM測定によって得られたピーク面積値の再現性を示す。SCAN測定では、SkatoleやButyric acidをはじめとして、全般的に変動係数が大きい値を示した。これは弱いピーク強度であったり夾雑成分からの影響を受けていることが推測される。一方SRM測定では、夾雑成分からの影響が抑えられ、且つ感度が向上したことにより、変動係数は0.1~8.6%と良好な再現性を示した。
Table 4 Repeatability of peak area by SCAN
| Compound | n = 1 | n = 2 | n = 3 | Ave. | STDEV | C.V.(%) |
|---|---|---|---|---|---|---|
| Acetic acid(m/z 60) | 26727058 | 23448580 | 30907431 | 27027690 | 3738502 | 13.8 |
| Isovaleric aldehyde(m/z 58) | 37894217 | 36797432 | 30177488 | 34956379 | 4174815 | 11.9 |
| Propionic acid(m/z 74) | 1118609 | 1169287 | 1238393 | 1175430 | 60128 | 5.1 |
| Isobutyric acid(m/z 73) | 441535 | 476884 | 494190 | 470870 | 26838 | 5.7 |
| Toluene(m/z 91) | 2066383 | 2268404 | 2248838 | 2194542 | 111419 | 5.1 |
| Butyric acid(m/z 60) | 540842 | 638348 | 465206 | 548132 | 86801 | 15.8 |
| Isovaleric acid(m/z 60) | 1623757 | 1962426 | 1671893 | 1752692 | 183223 | 10.5 |
| Valeric acid(m/z 60) | 505776 | 500742 | 414297 | 473605 | 51424 | 10.9 |
| Skatole(m/z 130) | 16467 | 10732 | 13107 | 13435 | 2882 | 21.4 |
Table 5 Repeatability of peak area by SRM
| Compound | n = 1 | n = 2 | n = 3 | Ave. | STDEV | C.V.(%) |
|---|---|---|---|---|---|---|
| Acetic acid(60→43) | 48198138 | 46441666 | 46676467 | 47105424 | 953573 | 2.0 |
| Isovaleric aldehyde(44→43) | 31611384 | 32652805 | 33453197 | 32572462 | 923531 | 2.8 |
| Propionic acid(74→55) | 1620757 | 1524801 | 1530497 | 1558685 | 53831 | 3.5 |
| Isobutyric acid(73→55) | 3658550 | 3502348 | 3510171 | 3557023 | 88012 | 2.5 |
| Toluene(91→65) | 8652579 | 8161044 | 8422329 | 8411984 | 245931 | 2.9 |
| Butyric acid(60→42) | 2326212 | 2132262 | 2092492 | 2183655 | 125049 | 5.7 |
| Isovaleric acid(60→42) | 4355087 | 4349861 | 4359477 | 4354808 | 4814 | 0.1 |
| Valeric acid(60→42) | 2327284 | 2243168 | 2132341 | 2234264 | 97776 | 4.4 |
| Skatole(130→77) | 50718 | 43135 | 44845 | 46233 | 3977 | 8.6 |
SRM測定によるValeric acidとSkatoleの確認
Fig. 3(a)にValeric acidとFig. 3(b)にSkatoleのSRMのクロマトグラムピークを示す。 SCAN測定で目的成分のマススペクトルが得られなかったValeric acidとSkatoleについては、複数のモニターイオン且つプリカーサーイオンとプロダクトイオンの関係から、観測されたピークが目的成分であると確認できる。
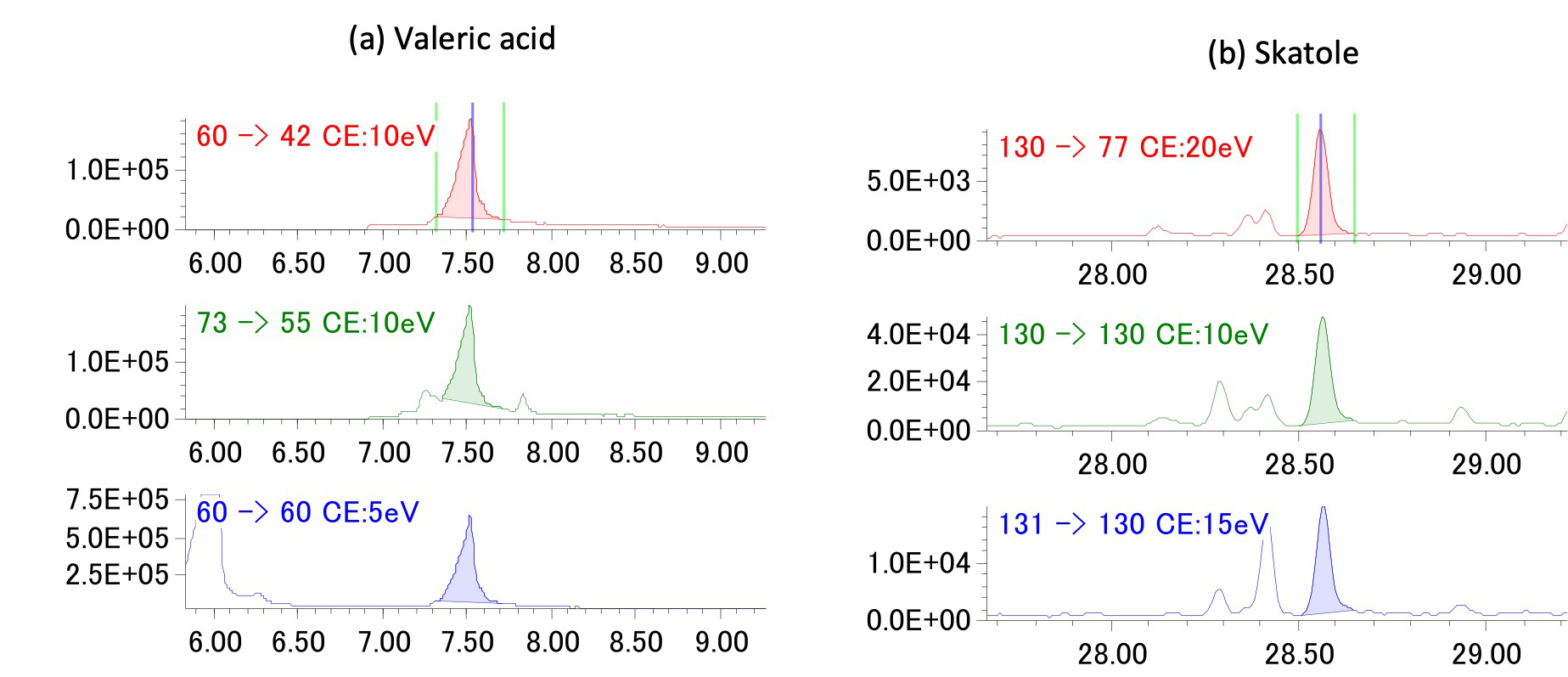
Fig. 3 SRM chromatogram peaks of valeric acid (a) and skatole (b)
まとめ
夾雑成分が多い材料中の異臭分析にはGC/MS/MSのSCAN/SRM測定が有効な測定方法となる。特に、JEOLのHSと組みわせたHS-GC/MS/MS測定は、より高感度分析が可能となるため、測定の試料量を減らすことができる。さらに、SRM測定は夾雑成分からの影響を抑える事ができると共に、SIM測定よりも多くのイオンを用いた測定となるため、微量成分の定性解析能力が向上する。それによって、より正確な測定を行うことができる。
謝辞
本アプリケーションノート作成にあたり、試料をご提供頂きました住友ゴム工業株式会社の海野様と吉谷様には感謝申し上げます。

