DioKを用いたポリ塩化ビフェニル(PCB)定量解析における塩素置換数の多い同族体からのフラグメントイオン由来ピークの識別方法
MSTips No.313
はじめに
ポリ塩化ビフェニル(PCB)は、昭和43年のカネミ油症事件をきっかけにその毒性が社会問題となり、製造や輸入が禁止となった。その後、平成13年に「ポリ塩化ビフェニル廃棄物の適正な処理の推進に関する特別措置法(通称:PCB措置法)」が施行され、PCB廃棄物の保管事業者は令和9年3月末までに低濃度PCB廃棄物を処分することが義務付けられた。
低濃度PCB廃棄物を分析する手法としては、「低濃度PCB含有廃棄物に関する測定方法」が環境省より示されている。令和元年10月に公表された第4版では、測定対象を塗膜くず(塩化ゴム系塗料や塩素系顔料)とする場合、ガスクロマトグラフ(GC)の検出器として使用できるものは質量分析計(タンデム型を含む)のみとなった。これは、塗膜くずが試料そのものに含塩素化合物を多量に含むため、電子捕獲型検出器(ECD)では適切な分析が困難となる場合が多いからである。
PCBは、塩素置換数により10種類の同族体に分けられる(Fig. 1)。電子イオン化(EI)においてPCBは塩素が脱離する開裂を起こす。そのため、ある同族体の定量イオン、確認イオンのクロマトグラム上に、それよりも塩素置換数の多い同族体からの脱塩素フラグメントイオン由来のピークが観測される。このフラグメントイオン由来のピークを定量計算に加えてしまうと定量値を過剰に見積もってしまうため、定量対象異性体と間違えないように確認しておく必要がある。
既報MSTips No.310 では、PCBの定量解析にダイオキシン分析プログラム「DioK(ダイオック)」が有用であることを報告した。DioKは、ピークごとに「異性体に対するアサインの『あり・なし』」及び「レシオチェック値の『許容値以下・以上』」の状態を色分けして表示することができ、該当する同族体由来のピークであるか否かを判定しやすい。今回は本機能を使用した塩素置換数の多い同族体からのフラグメントイオン由来ピークの識別方法を紹介する。
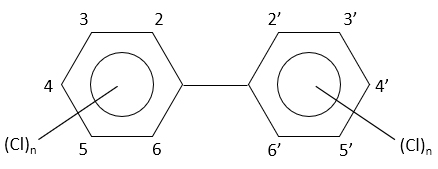
Fig. 1 PCBs basic structural formula
実験
測定試料はカネクロール混合液(KC-mix、ジーエルサイエンス社製 100 μg/mL)をヘキサンで5μg/mLに希釈した溶液を用いた。測定にはガスクロマトグラフ四重極型質量分析計 JMS-Q1500GC を使用し、測定条件は「絶縁油中の微量PCBに関する簡易測定法マニュアル(第3版)」を参考に設定した(Table 1)。
また、一塩化ビフェニル(M1CB)から十塩化ビフェニル(D10CB)のSIM測定における定量イオン(Quantitation ion)と確認イオン(Confirmation ion)をTable 2に示した。SIM測定の結果は、DioKで解析した。一般的なPCBの定量ではScan測定は必要ないが、今回はPCBのフラグメントイオンのマススペクトルを示すためにScan測定も実施した。
Table 1 Measurement condition
| GC | |
|---|---|
| Column | DB-5ms(Agilent Technologies, Inc.) 30m×0.25mm I.D., df=0.25µm |
| Injection port temp. | 250°C |
| Oven temp. program | 100°C(1min)→20°C/min→160°C→3°C/min →220°C(3min)→ 6°C/min→295°C(5min) |
| Injection mode | Splitless |
| Carrier gas | He, 1.2mL/min(Constant Flow) |
| MS | |
| Ion source temp. | 230°C |
| Interface temp. | 280°C |
| Ionization mode | EI |
| Ionization energy | 70eV |
| Ionization current | 50µA |
| Mesurement mode | Scan, SIM |
| Relative EM Voltage | 700V |
Table 2 Selected ions of each target PCB substance
| M1CB | D2CB | T3CB | T4CB | P5CB | H6CB | H7CB | O8CB | N9CB | D10CB | ||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Native (m/z) |
Quantitation ion | 188.0 | 222.0 | 256.0 | 289.9 | 325.9 | 359.8 | 393.8 | 429.8 | 463.7 | 497.7 |
| Confirmation ion | 190.0 | 224.0 | 258.0 | 291.9 | 323.9 | 361.8 | 395.8 | 427.8 | 461.7 | 499.7 | |
| Internal Standard (m/z) |
Quantitation ion | 200.1 | 234.0 | 268.0 | 302.0 | 337.9 | 371.9 | 405.8 | 441.8 | 475.7 | 509.7 |
| Confirmation ion | 202.1 | 236.0 | 270.0 | 304.0 | 335.9 | 373.9 | 407.8 | 439.8 | 473.7 | 511.7 | |
結果
H6CBの定量対象異性体の平均同族体クロマトグラムと、DioKのテンプレート内に登録されているリテンションタイムをFig. 2に示す。既報MSTips No.310 で報告したように、DioKではレシオチェックが許容値内(マニュアルでは20%以下)で異性体としてアサインされているピークは緑色で表示されるため、H6CBの異性体ピークであることがわかる。水色と青色のピークは、冒頭で述べたように塩素置換数の多い同族体のフラグメントイオンの影響である可能性がある。
そこで、Fig. 3にH6CB、H7CB、O8CBの定量対象異性体の平均同族体クロマトグラムを並べてみた。これをみると、H6CBの平均同族体クロマトグラム上の青色及び水色のピークと同じリテンションタイムにH7CBとO8CBのピークが存在することが分かる。したがって、青色と水色のピークは塩素置換数の多い同族体のフラグメントイオン由来と識別できる。次ページにH6CB、H7CB、O8CBのマススペクトルの一例を示し、これらを識別できる理由を説明する。
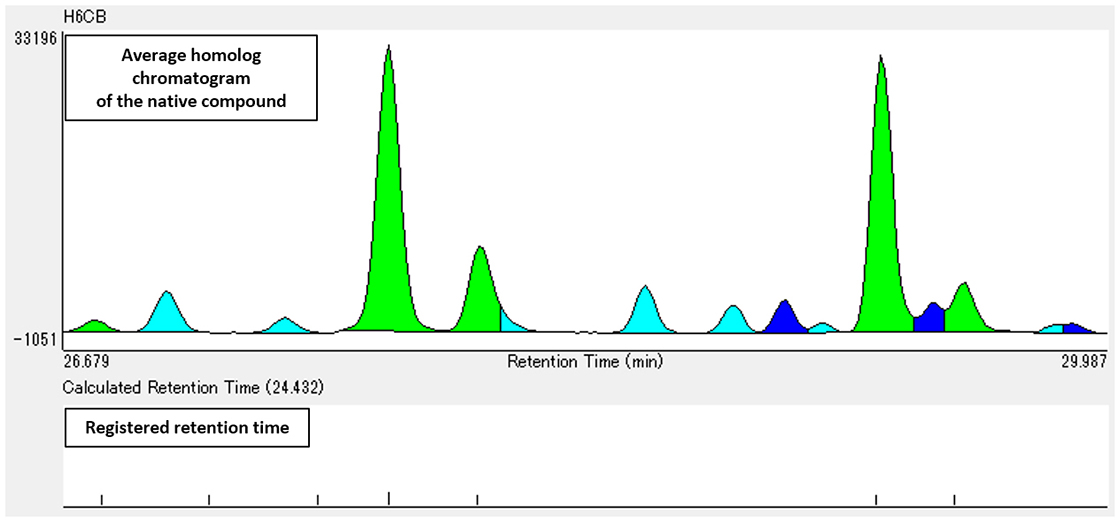
Fig. 2 Average homolog chromatogram of the native compound and registered retention time(H6CB)
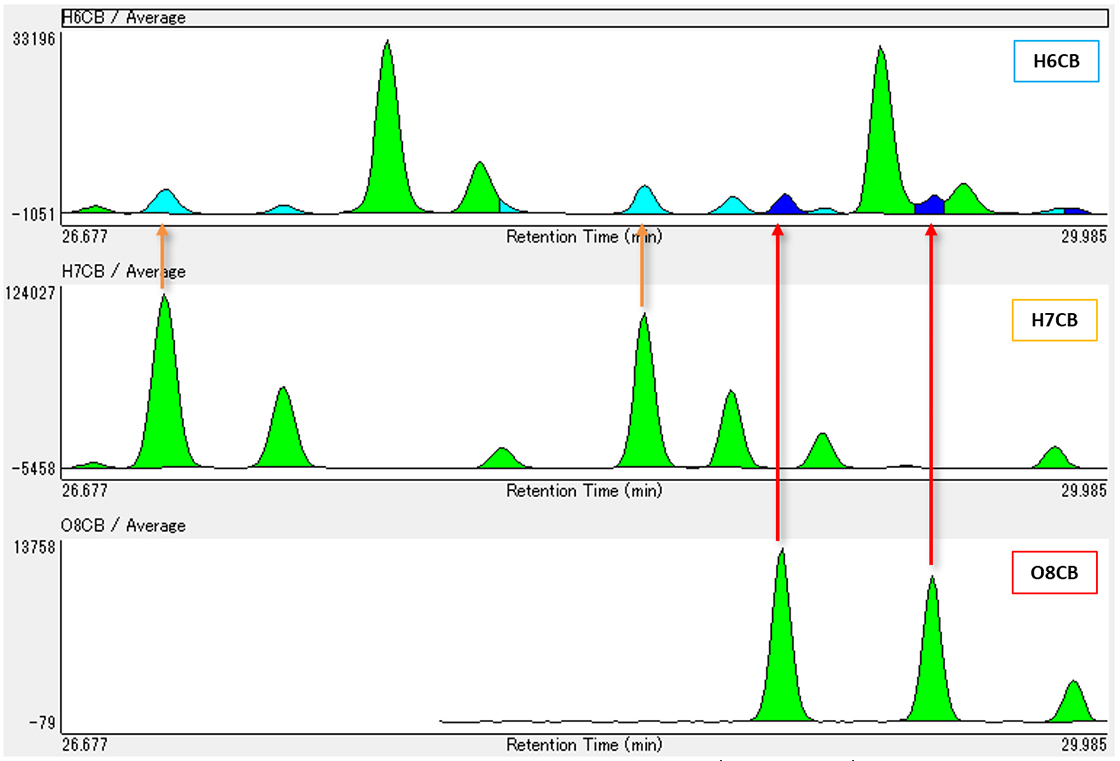
Fig. 3 Average homolog chromatograms of the native compound (H6CB, H7CB, O8CB)
H6CB、H7CB、O8CBのマススペクトルをFig. 4に示す。それぞれのマススペクトルにおいて、一番高質量側のピーク群が分子イオン(M+・)である。塩素置換数の多い同族体の脱塩素フラグメントイオンは、置換数の少ない同族体の分子イオンと近いm/zに観測されることがわかる。Fig. 4には、それぞれの同族体のm/z 360付近を拡大したマススペクトルをあわせて示した。H7CBとO8CBの脱塩素フラグメントイオンは水素置換数が少ない分、H6CBの分子イオンに対して低質量側に1および2uシフトしている。
なお、H7CBとO8CBのフラグメントイオンはそれぞれの妨害の仕方が異なるため、H6CBにおけるレシオチェックの結果に違いが見られる。H6CBの分子において定量イオン(m/z 360)と確認イオン(m/z 362)の分子組成はそれぞれ「12C12 1H4 35Cl5 37Cl」と「12C12 1H4 35Cl 37Cl2」である。H7CBからの脱塩素フラグメントイオンはHが1つ少ないため、m/z 360とm/z 362に現れるピークの分子組成としては、「12C11 13C 1H3 35Cl5 37Cl」と「12C11 13C 1H3 35Cl4 37Cl2」となる。レシオチェックに影響をあたえるのは35Clと37Clの数の比であり、H6CBとH7CBではその比が一致していることからレシオチェックはOK(ピークの色が水色)となる。
この場合、レシオチェックの結果だけでは定量対象異性体かフラグメントイオン由来のピークか識別できないので、各同族体リテンションタイムの情報(登録リテンションタイム)が重要となる。一方O8CBからの脱塩素フラグメメントイオンは、Hが2つ少ないため、m/z 360とm/z 362に現れるピークの分子組成は、「12C12 1H2 35Cl4 37Cl2」と「12C12 1H2 35Cl3 37Cl3」となる。H6CBとO8CBでは、35Clと37Clの数の比が異なるため、レシオチェックはNG(ピークの色が青色)となりレシオチェックにより識別することができる。 以上より、DioKを使用することで、塩素置換数が1多い同位体からのフラグメントイオン由来のピークは、実測のリテンションタイムと登録リテンションタイムを比較することで識別することが可能である。
また、塩素置換数が2多い同位体からのフラグメントイオン由来のピークは、DioK 上では色分けにより区別されている「定量イオンと確認イオンのクロマトグラム上のピーク面積比(レシオチェック)」を確認することで容易に識別することが可能である。
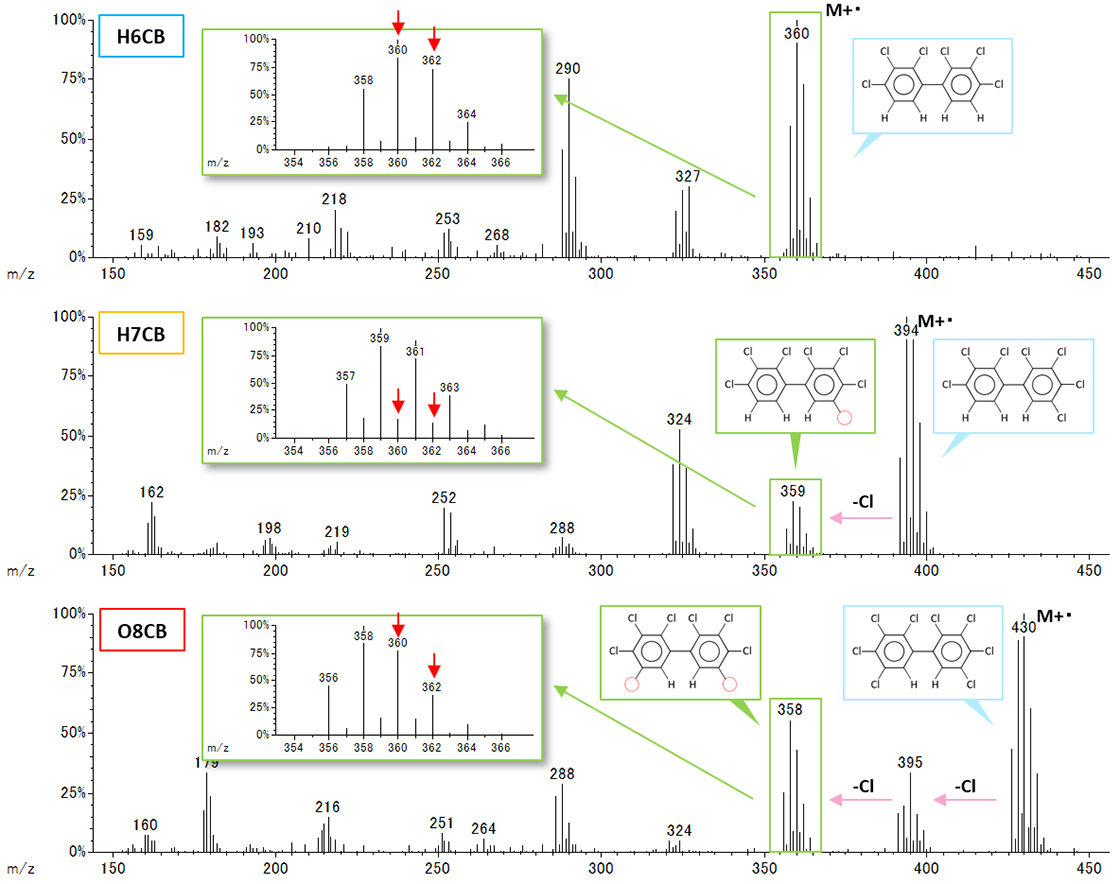
Fig. 4 Mass spectra of H6CB, H7CB, and O8CB
まとめ
本報告では、塩素置換数の多い同族体からのフラグメントイオン由来ピークの識別方法について紹介した。フラグメントイオン由来のピークを定量計算に加えてしまうと定量値を過剰に見積もってしまうため、定量対象異性体と間違えないように注意する必要がある。
DioKを用いたPCBの定量解析では、ピークの色と登録リテンションタイムの表示により、定量対象異性体かフラグメントイオン由来のピークかを判断することができる。さらに、同一画面上に塩素置換数の異なる同族体クロマトグラムを表示させることもできるため、詳細な確認も可能である。
参考文献
「低濃度PCB含有廃棄物に関する測定方法(第4版)」. 環境省 環境再生・資源循環局 廃棄物規制課 ポリ塩化ビフェニル廃棄物処理推進室. 令和元年10月.「絶縁油中の微量PCBに関する簡易測定法マニュアル(第3版)」.環境省大臣官房廃棄物・リサイクル対策部産業廃棄物課. 平成23年5月.
- このページの印刷用PDFはこちら。
クリックすると別ウィンドウが開きます。 
PDF 700KB
