ESRによるイオウラジカルの測定 – 環境中有害物質との反応 –
ER200001
近年、生体内で強い還元性を持つ活性イオウと呼ばれるパースルフィド (R-SSH)、ポリスルフィド (R-SSSH, ;R-SSSSH) 等のイオウ化合物が注目されています。既にESRアプリケーションノート; ER190011 で報告したように、こうした活性イオウはキノン化合物と反応してキノンラジカルを生成します。
環境中のディーゼル排気ガス中微粒子に含まれる9,10-Phenanthraquinone (PQ) もキノン化合物の一つです。これは、生体内酵素のP450-Reductaseにより溶存酸素から活性酸素 (Reactive oxygen speicis ;ROS) の一種であるSuperoxide anion radical (O2・-) を生成する1) ことを、アプリケーションノート ER150007 でご紹介しました(図1参照)。
O2・-は極めて活性の高いHydroxy radical (HO・) に変換されるため、これがPQの毒性の要因と考えられます。今回は、PQが活性イオウ共存下で非酵素的に起こす反応をESRにより検討しました2)
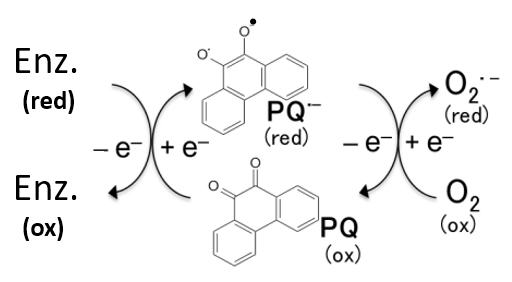
図1.PQは酵素反応により活性酸素を生成する
試料と測定装置
1. 試薬
1) イオウ化合物
活性イオウ- Na2S2 (Na-SS-Na)
- Na2S3 (Na-SSS-Na)
- Na2S4 (Na-SSSS-Na) 全て同仁化学研究所製
- Dithiothreitol (DTT) 同仁化学研究所製
- Na2S (Na-S-Na) 同仁化学研究所製
- Glutathione (GSH) Sigma-Aldrich 社製
2) キノン化合物
- PQ ; 99.9% Sigma-Aldrich社製
2. 測定装置
1) 溶存酸素測定計 B-505(飯島電子工業社製)で反応溶液中の溶存酸素 (dissolved oxygen) を測定
2) ESR JES-X320(日本電子社製)で反応液中のラジカルを測定
(測定条件はESRアプリケーションノート;ER190011 に準じた)
別途、Na2S2濃度を1/10としてスピントラップ剤;DMPOによるトラップ実験を行った
結果
1. 溶存酸素測定
PQを、各種活性イオウと混合すると速やかに溶存酸素が減少することが確認されました(図2)。
この現象は、モノチイル化合物との混合および活性イオウ単独では認められなかったことから、活性イオウは非酵素的にPQと酸素を利用した反応を生じることが示唆されました。
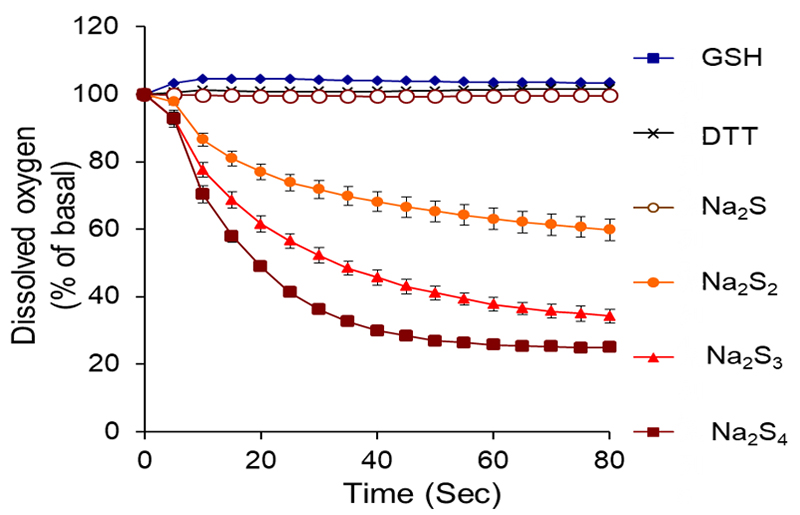
図2. PQと各種イオウ化合物混合後の溶存酸素量の経時変化
2.PQと活性イオウのラジカル検出
PQと各種活性イオウを混合したところ、全てのケースで2種類のラジカルが検出されました。
図3に、Na2S2と混合して得られたESRスペクトルを示しました。Mnマーカーを基準として得られたg値から、活性イオウラジカル(g=2.0015)およびPQ由来セミキノンラジカル(g=2.0045)と同定されました。
しかし、モノチイル化合物との混合ではこのようなラジカルは得られませんでした。
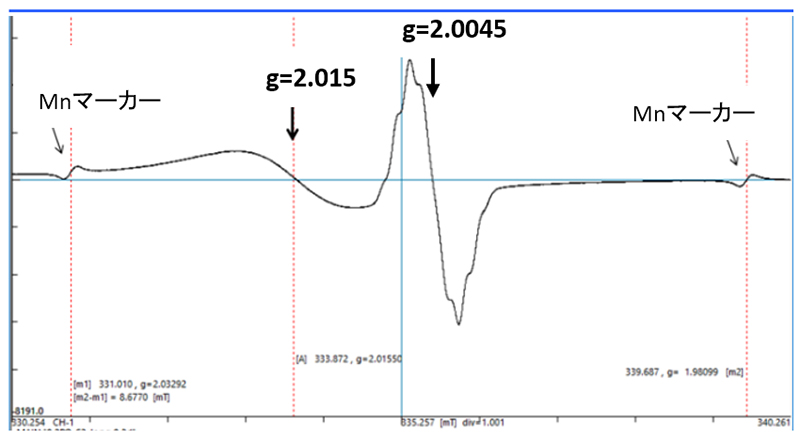
図3. PQとNa2S2混合して3分後に得られたESRスペクトル
3.O2・-の検出
O2・-の検出を試みましたが、実験2.の条件ではDMPOアダクトは検出されませんでした。
活性イオウによる還元性に起因すると考え、Na2S2濃度を1/10としたところ、図4に示したスペクトルが得られました。活性イオウとPQの無い条件では、信号は得られませんでした。
75%-Acetoneという溶媒環境のため、水溶液中とは異なる分裂を示しましたが、これまでの結果を合わせ、O2・-とHO・のDMPOアダクトが混在している(DMPO-ROSと表記)と考えられました。
活性イオウはPQと反応し活性酸素を生成することが示唆されました。
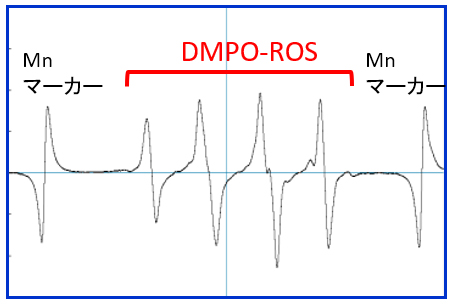
図4. 低濃度Na2S2 + PQ溶液から得られたDMPOアダクトのESRスペクトル
まとめ
活性イオウは、PQと非酵素的に反応し、電子の授受を行うことが示唆されました。反応経路を図5のように推定しました。
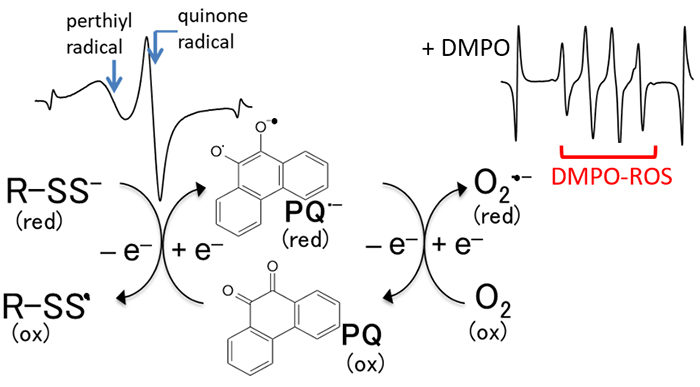
図5. PQと活性イオウの反応経路(推定)
参考文献
- Kumagai Y. et al. Chem. Res. Toxicol. 15:483-489, 2002
- Abiko Y. et al. Chem. Res. Toxicol. 32(4):551-556, 2019
- このページの印刷用PDFはこちら。
クリックすると別ウィンドウが開きます。 
PDF 620KB
