COSY/TOCSYの解析│2D NMRでスピン相関を読み解く
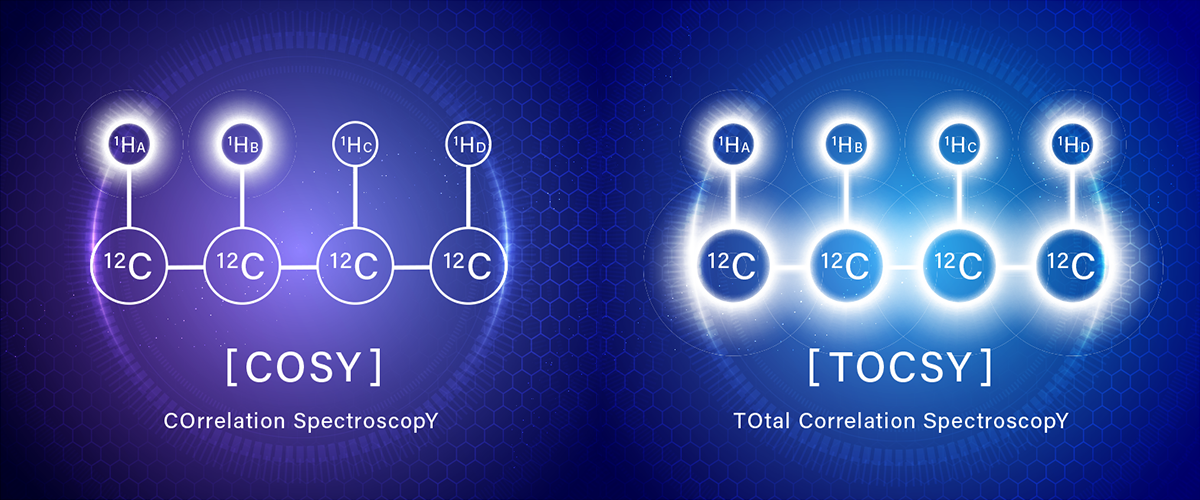
本コラムでは、2D NMRの代表的手法であるCOSY、TOCSYの基礎原理と解析方法を解説します。COSYによる隣接する1H同士の相関の確認から、TOCSYによるスピンネットワーク解析、1D・2D TOCSYによる糖類解析を、具体例を交えて紹介します。さらに、各手法の特徴や使い分けもわかりやすくまとめていきます。
COSYとは
COSY(COrrelation SpectroscopY)は、隣接する1H同士のカップリングを2次元NMRで可視化する基本手法です。従来は、1H同士のホモデカップリングを利用して、隣り合う1H原子同士を1つずつ探していましたが、COSYの登場により広帯域で複数の結合相関を同時に解析できるようになり、構造解析の効率が飛躍的に向上しました。現在では、1H-1H 相関を確認する入門的な2D NMR測定法として広く利用されています。
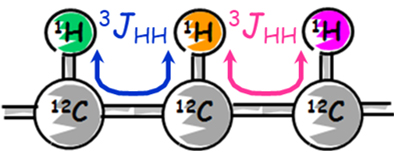
COSYは、隣接する1H同士、つまり、3結合離れた1H同士の相関が現れます。
3結合離れたスピン結合を、3JHHと表します。
隣り合う1Hが分かれば、分子構造内での1Hのつながり方が分かります。
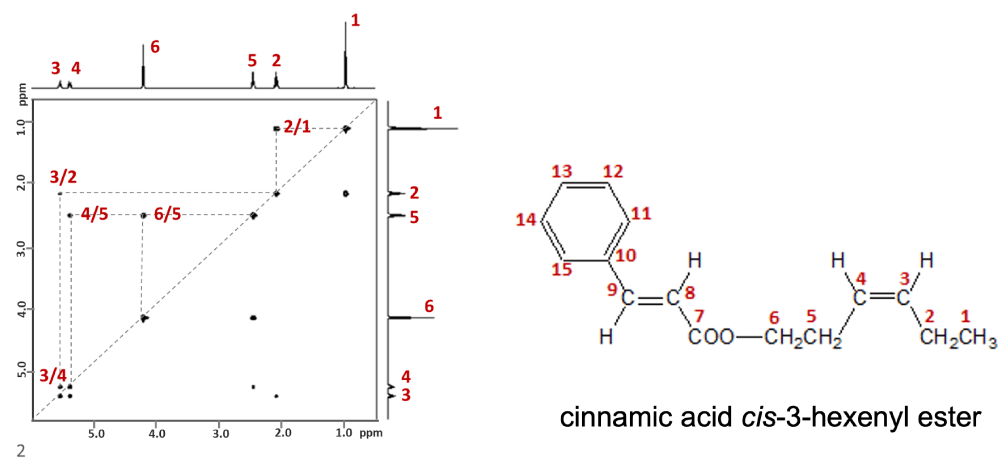
図1 cinnamic acid cis-3-hexenyl esterのCOSYスペクトル
図1は、「cinnamic acid cis-3-hexenyl ester」の1~6の1Hに相当する領域のCOSYスペクトルです。
上図のように、相関信号と両軸の1Dの1Hスペクトルを繋ぐと、1-2、2-3、3-4、4-5、5-6の5つの相関が観測され、その結果から、1~6までの1H同士が、それぞれ隣接した構造を有していることが推測できます。
また、COSYでは、隣り合う1H間のカップリング情報から、間接的に炭素原子同士のつながりも分かり、これらの情報は、部分構造を求める上でとても重要です。
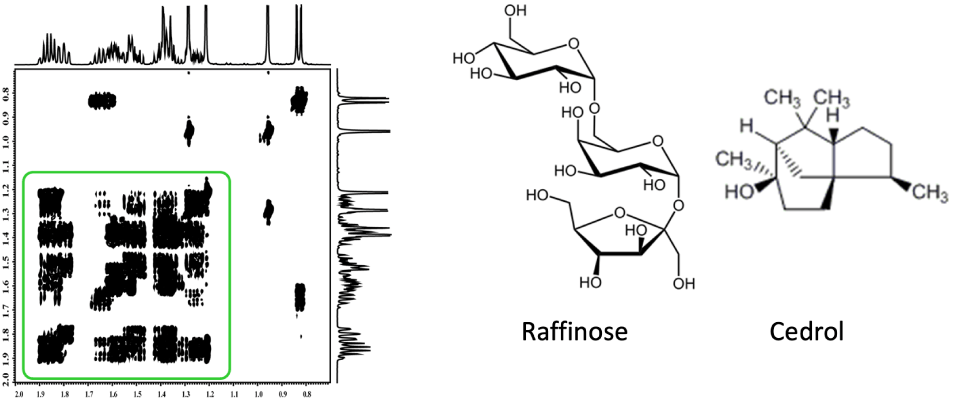
図2 複雑なCOSYスペクトル
しかし、図2のような複雑なCOSYスペクトルの場合はどうでしょうか。
緑で囲んだ領域を見ると、信号が重なり合い、相関を認識するのが容易ではないことが分かります。これでは、構造決定を先に進めることができそうにありません。
図2のような1Hの信号が、狭い範囲に密集して現れる 多糖類や、環状の化合物では、COSYスペクトル情報のみでは、構造解析が行き詰ってしまうことがあります。
COSYで、十分な解析ができない場合の一つの解決策がTOCSYです。
次章からTOCSYについて解説いたします。
TOCSYとは
TOCSY(TOtal Correlation SpectroscopY)は、同じスピンネットワークに属するすべての1Hを2次元NMRで一括して可視化できる手法です。スピン結合は連鎖的に伝播するため、隣接した箇所だけでなく、スピン系全体の相関が取得でき、複雑な有機分子や糖・アミノ酸の解析に有効です。TOCSYは 、HOHAHA(HOmonuclear HArtmann-HAhn spectroscopy) とも呼ばれ、基本的に同一の測定法を指します。
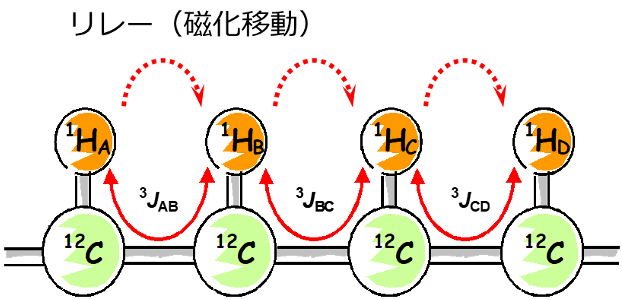
図3 連続した1Hのスピン結合のネットワーク
例えば、図3に示すような原子のつながりがあるとします。
HA・HB・HC・HDは、それぞれ隣接した1H同士がスピン結合でつながっており、このつながりをスピン系(スピンネットワーク)といいます。
スピン系は、Hの付加されていない四級炭素や、酸素を介して結合した1Hには、伝播できず、途切れてしまいます。
TOCSYでは、同じスピン系の中にある直接スピン結合のない核スピン間(例: 1HA - 1HD )の相関を見ることができます。
TOCSYでは、HAの磁化をHBに移して、HBに移った磁化をHCに移し、HCに移った磁化を、さらにHDに移していきます。つまり、磁化を、スピン系内で、どんどん移動し、繋げていくということを行っています。
この磁化移動を「リレー」と呼び、TOCSYでは、このリレーによる相関信号を観測します。
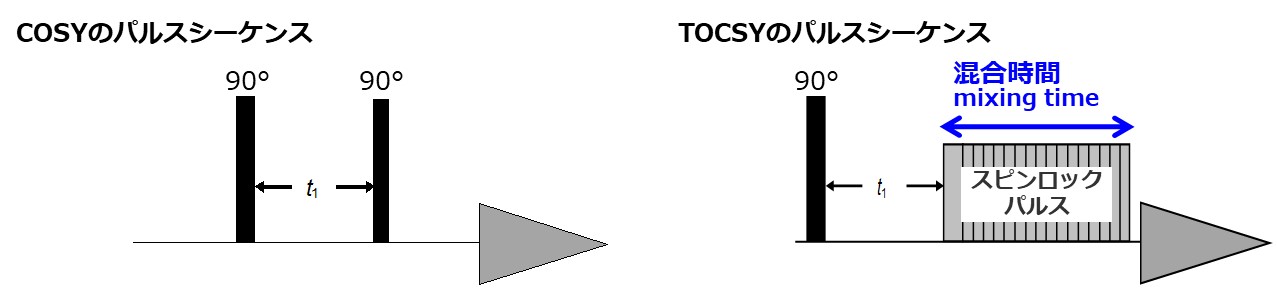
図4 COSYとTOCSYのパルスシーケンス
図4はCOSYとTOCSYのパルスシーケンスです。 COSYでは、2つの90°パルスを使っていますが、TOCSYでは、2つ目のパルスがスピンロックパルスになります。 このスピンロックパルスをかける時間を『混合時間』といい、 TOCSYでの重要なパラメータとなります。 混合時間を長くすることで、より遠くまでリレーされた相関信号を観測することができます。
TOCSYの混合時間と相関信号
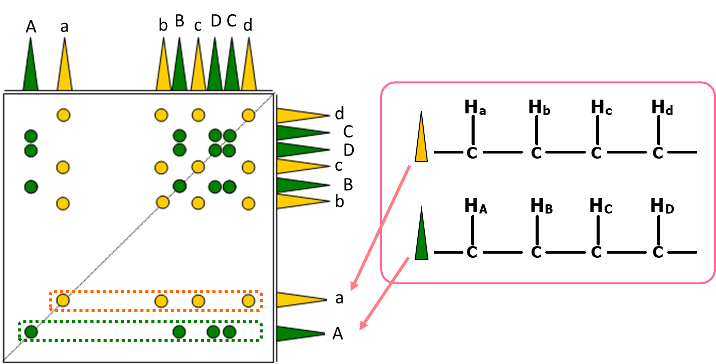
図5 TOCSYスペクトルの模式図
図5は、2つの独立したスピンネットワークを有する化合物のTOCSYスペクトルを模式的に表したものです。それぞれのスピンネットワークを黄色と緑で示しています。このようにTOCSYでは、
それぞれのスピンネットワークに属するすべての1Hの相関が観測されます。
このとき、両軸の一次元スペクトル内の信号『A』と『a』のように、信号の密集した領域から離れた位置で現れる信号があれば、黄色と緑で分類されたネットワークのように、別々に分類し、それぞれのスピンネットワークを確認することが容易になります。
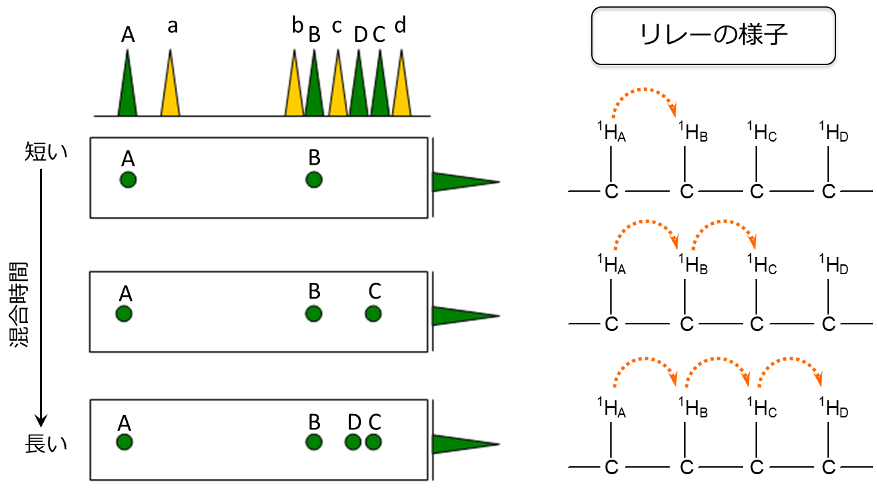
図6 TOCSYの模式図(Aの相関)
次に混合時間を変えたときのAの相関信号の変化を見てみます。
図6は、図5のTOCSY模式図のAの相関を拡大したものです。
短い混合時間では、1HAの磁化は、隣の1HBにのみ移動し、 1HB との相関信号Bが現れます。
さらに混合時間を長くすると、磁化は、1HCに移動し、相関信号Cが現れます。
さらに、さらに混合時間を長くすると、磁化は、1HDまで移動し、相関信号Dが検出され、結果として、 1HA - 1HB - 1HC - 1HDのつながりを持っていることが分かります。
混合時間が長いほど、より遠くまで磁化が移動するため、十分に長い混合時間を取ると、磁化を、同じスピン系に存在するすべての1Hまで移動させることができ、同じスピン系に存在するすべての1Hの相関信号を得ることができます。
また、混合時間を変化させたスペクトルを比較することで、1Hの繋がっている順番も知ることができます。
2D TOCSYによるスクロースの解析例
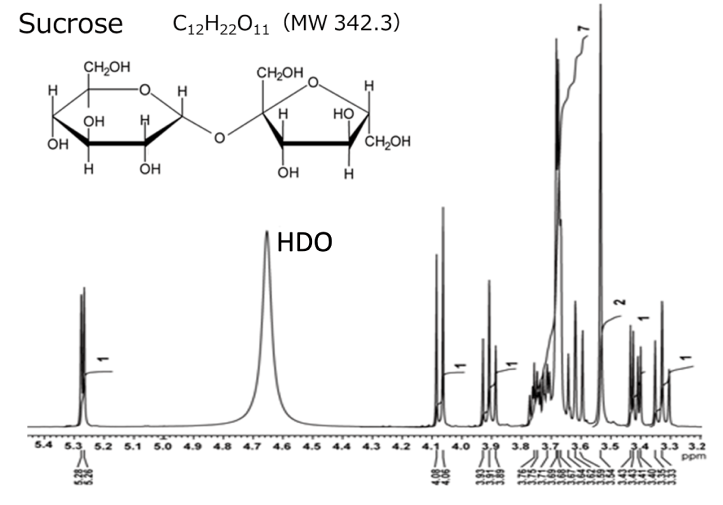
20 mg / 0.6 mL D2O溶液(400 MHz)
ここからは、2D TOCSYによるスクロース解析例をご紹介します。 スクロースは、グルコースとフルクトースがグリコシド結合で結合した二糖です。 スクロースは、全部で22個の1Hを有していますが、サンプルは重水に溶解しているため、水酸基(-OH)の1Hは重水素交換により、観測されていません。 したがって、ここでは、8個の水酸基の1Hを除いた14個の1Hが観測されています。
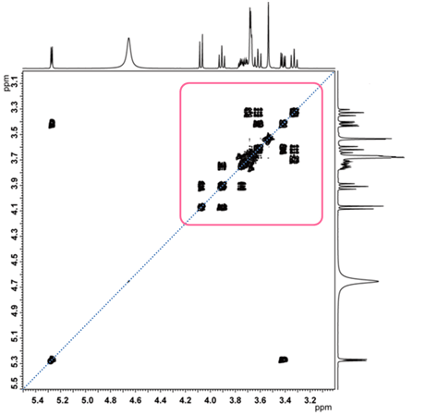
図7 スクロースのCOSYスペクトル
はじめに、スクロースのCOSYスペクトルを図7に示します。
赤枠で囲んだ部分を拡大して、図8に表示します。
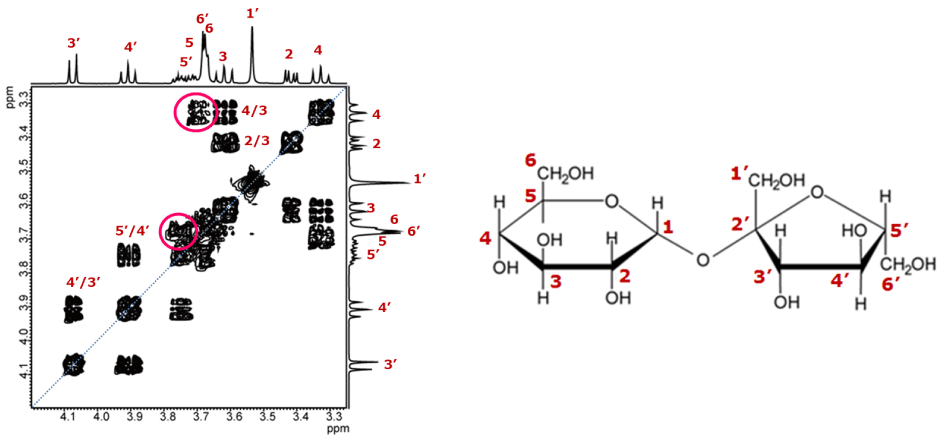
図8 スクロースのCOSYスペクトル
まず、図7で、6つの相関信号を、比較的簡単に見つけることができます。
ところが、図8の赤丸で示されるような化学シフトの接近しているエリアに現れる信号の相関を読み取るのは難しく、ここで解析作業に行き詰ってしまう人が多いでしょう。
そこで、TOCSY法を使ってみることにします。
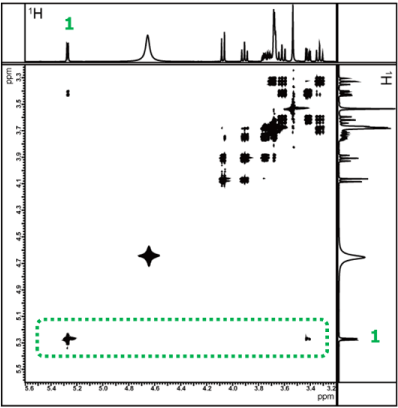
混合時間を20msに設定した
TOCSYスペクトル
混合時間を150msに設定した
TOCSYスペクトル
図9 混合時間を 20 ms と 150 ms に設定して測定したTOCSYスペクトル
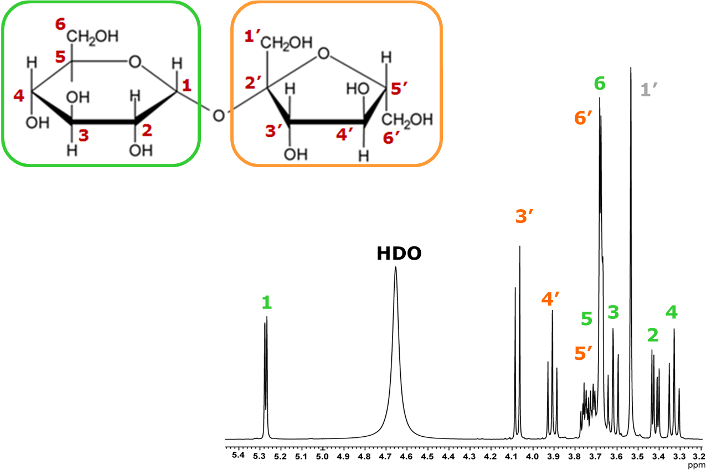
混合時間を 20 ms と 150 ms にそれぞれ設定し、測定したTOCSYスペクトルを図9に示します。
まずはじめに、他の信号から化学シフトの離れた位置に現れるグルコースの1位の1Hの相関信号に注目します。
先ほど図6で示したように、混合時間を変えたときの相関信号の変化を見て、1位の1Hからのリレーを確認していきます。
混合時間を長くすると、多くの相関信号が現れていることも見て取れます。
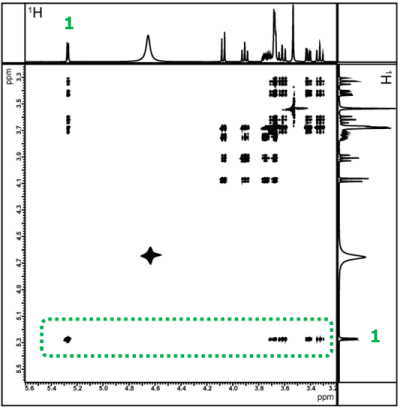
また、信号が重なった領域は、二次元スペクトルで見るよりも、スライスデータで比較した方が分かりやすいので、 1位の1Hの相関信号をX軸に沿って(緑の枠のエリアで)切り出した一次元スペクトルで、比較することにします。
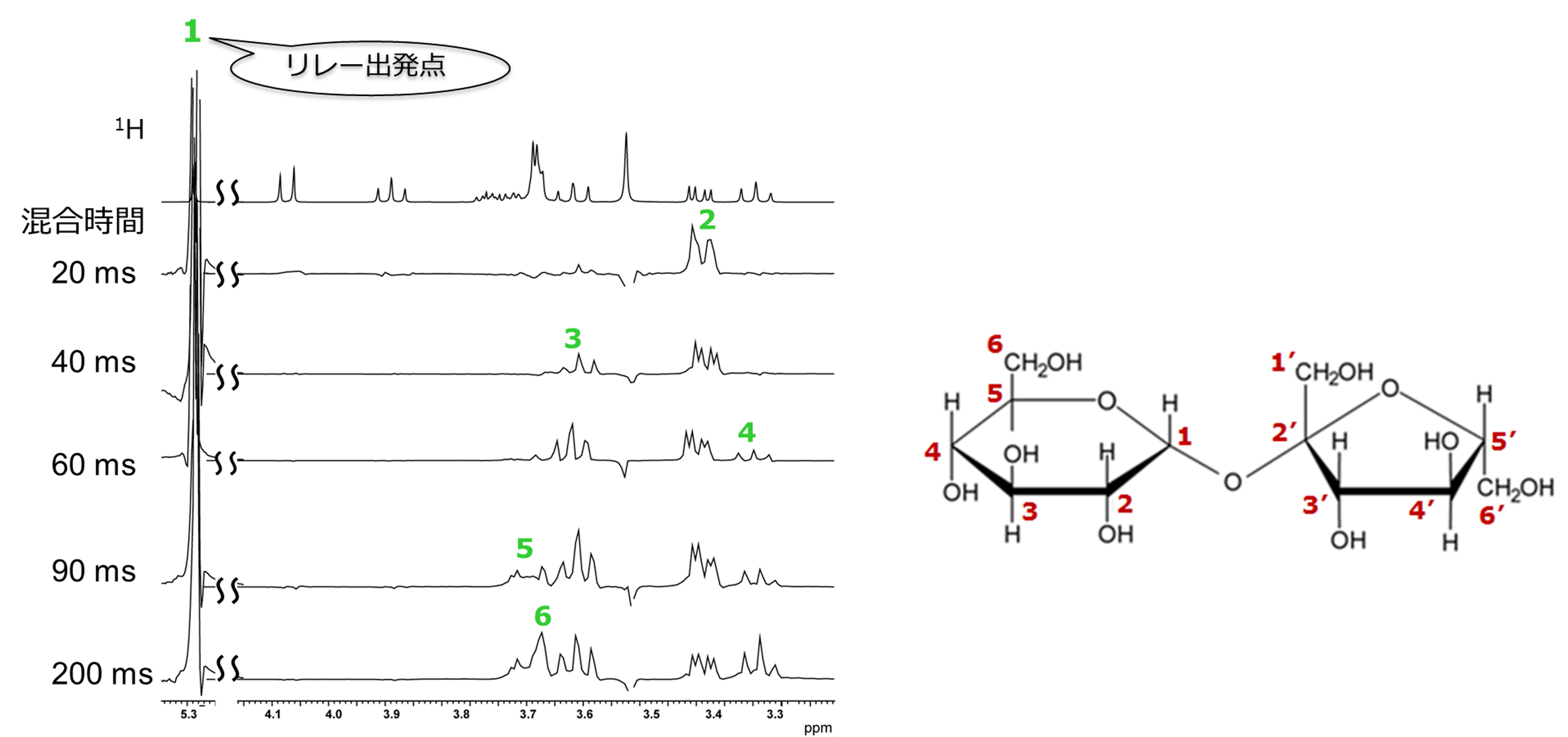
図10 スクロースの1位1Hの相関信号をX軸に沿って切り出した一次元スペクトル
図10の一番上は、通常の1Hスペクトルです。その下に、混合時間を 20 msから200 msまで変えたスライスデータを並べてあります。
左の信号が1位の1Hで、これをリレーの出発点と考えます。
混合時間 20 ms では、隣にある2位の1Hとの相関だけが現れ、1と2のつながりのみがわかります。
混合時間を長くしていくと、相関信号が順々に現れ、最終的にグルコースの部分の1位から6位までのつながりを確認することができます。
COSYでは、5位の1Hの相関の相手を明確に読み取ることは困難でしたが、TOCSYでは、その情報を得ることができました。
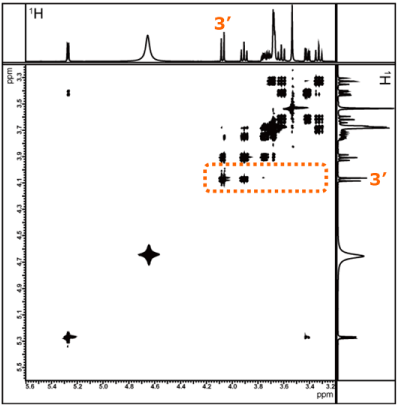
つぎは、フルクトースの3'位の1Hを出発点としたリレーを確認してみましょう。
スクロース部位の測定と同様に、混合時間を変えたときのTOCSYスペクトルを図11に示します。
混合時間を20msに設定した
TOCSYスペクトル
混合時間を150msに設定した
TOCSYスペクトル
図11 混合時間を 20 ms と 150 ms に設定して測定したTOCSYスペクトル
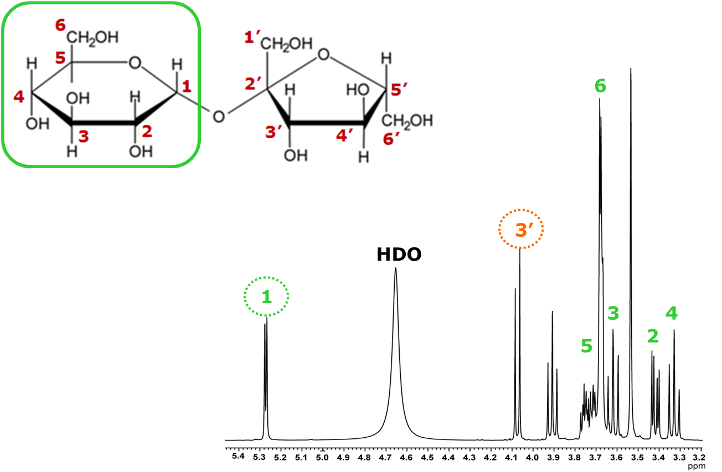
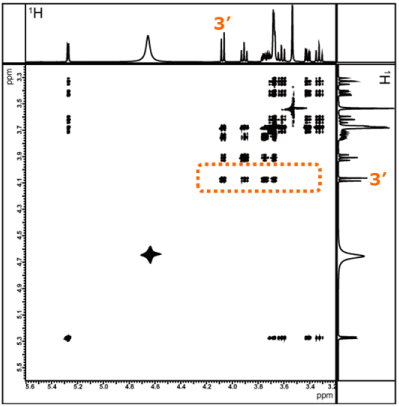
先ほどと同様に、信号が混み合っていない位置に現れる信号(今回は、フルクトースの3'位の1Hに着目)の、X軸方向のスライスデータを比較します。
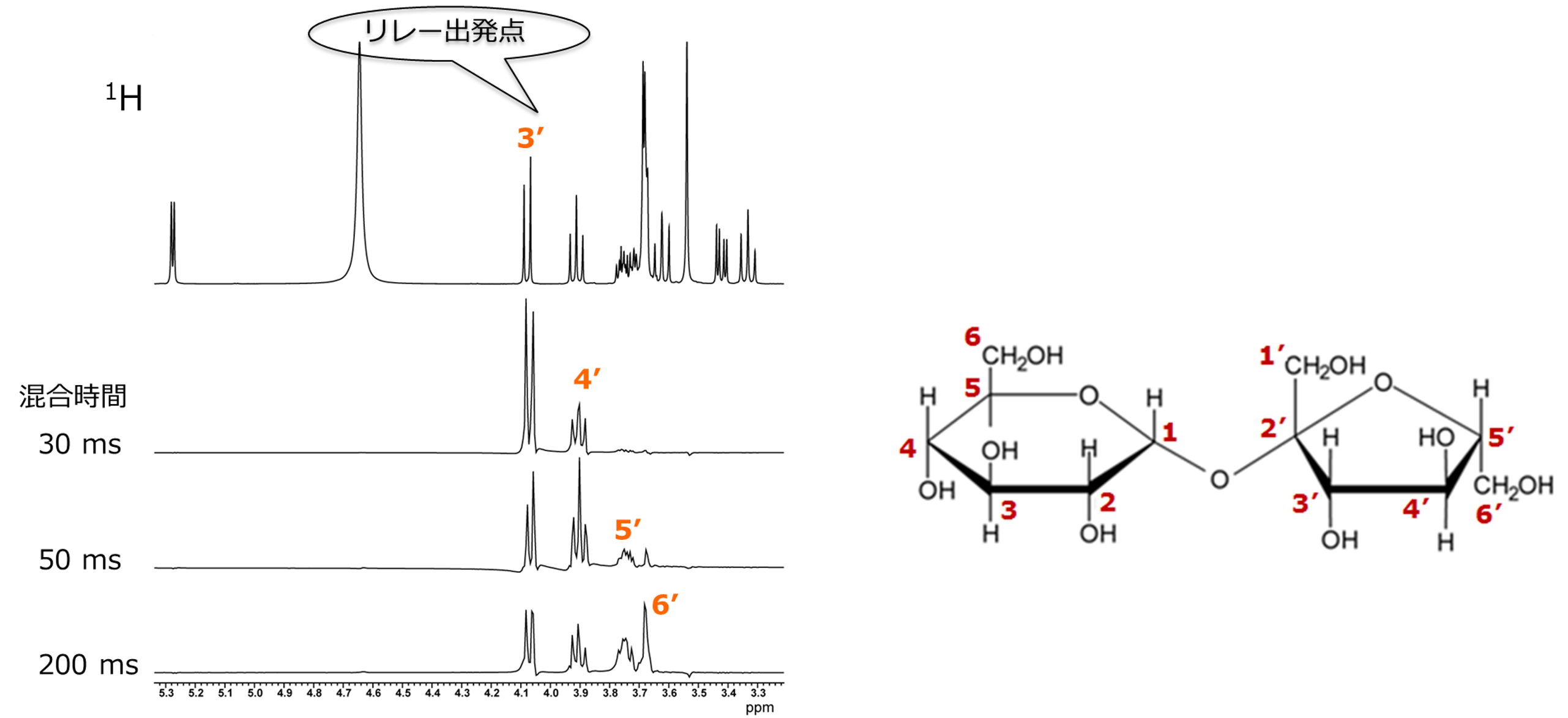
図12 フルクトースの3位1Hの相関信号をX軸に沿って切り出した一次元スペクトル
図12の一番上は、通常の1Hスペクトルで、下には、混合時間を変えたときのスライスデータを並べたました。
先ほどと同じように、3'位の1Hをリレーの出発点とし、混合時間を長くしていくと、4'位, 5'位, 6'位の1Hとの相関が現れ、フルクトース部分のつながりも確認することができました。
このように、TOCSYを利用すると、複数のスピンネットワークを含む化合物のスピンネットワークを別々に取り出すことができます。また、混合時間を変えることで、起点とした1Hのからの距離も確認することができます。 COSYスペクトルが複雑になってしまっても、TOCSYを利用すれば、分子構造を決定する大きなアシストを得ることができます。
1D TOCSYによるグルコースの解析例
1D TOCSY は 、2D TOCSY の一次元版で、基本的な原理は同じです。
2D TOCSY が、分子全体のスピンネットワークを把握するために用いられるのに対し、 1D TOCSY は、特定の1Hが属するスピン系のみを確認したい場合により有効です。 1D TOCSYでは、選択的に励起した1Hからの磁化移動、すなわちリレーの様子を観測します。混合時間を段階的に延長することで、スピンネットワークに沿った磁化リレーの伝播過程を追跡できます。選択励起には、他のシグナルから化学シフトが十分に離れた1Hを用いるとよいでしょう。また、1D 測定は、 2D 測定に比べて、デジタル分解能が高く、信号の重なりを回避しやすい点も利点です。
それでは、実際に、グルコースの解析を例にご紹介します。
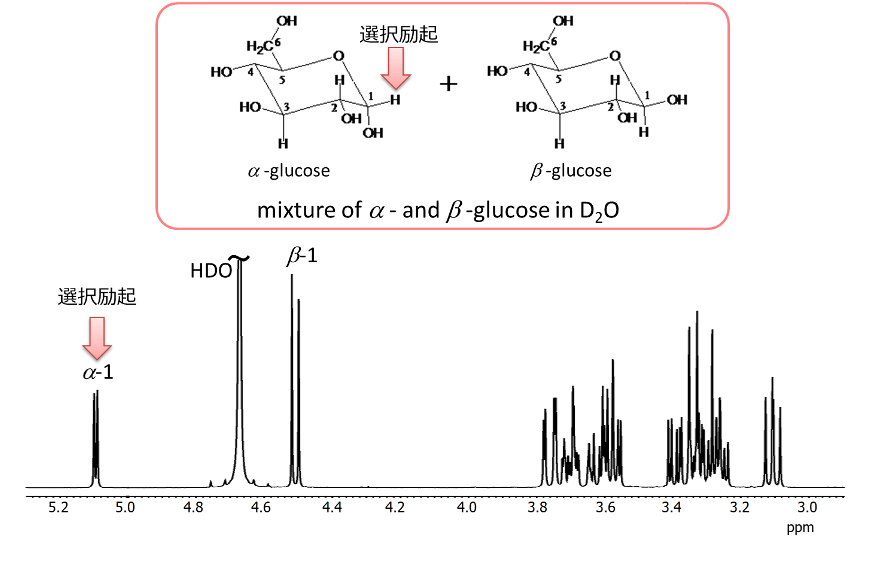
図13 グルコースの1Hスペクトル
グルコースは、水溶液中では、α型とβ型のアノマー体として存在しています。そのため、1Hスペクトルは、図13に示すように、αグルコースとβグルコースの混合スペクトルとなります。 選択励起する1Hについては、糖の場合、1位のアノメリック1Hなど、他より低磁場にある1Hを選びます。 αグルコースの1位のアノメリック1Hを選択励起した1D TOCSYの結果を、図14に示します。
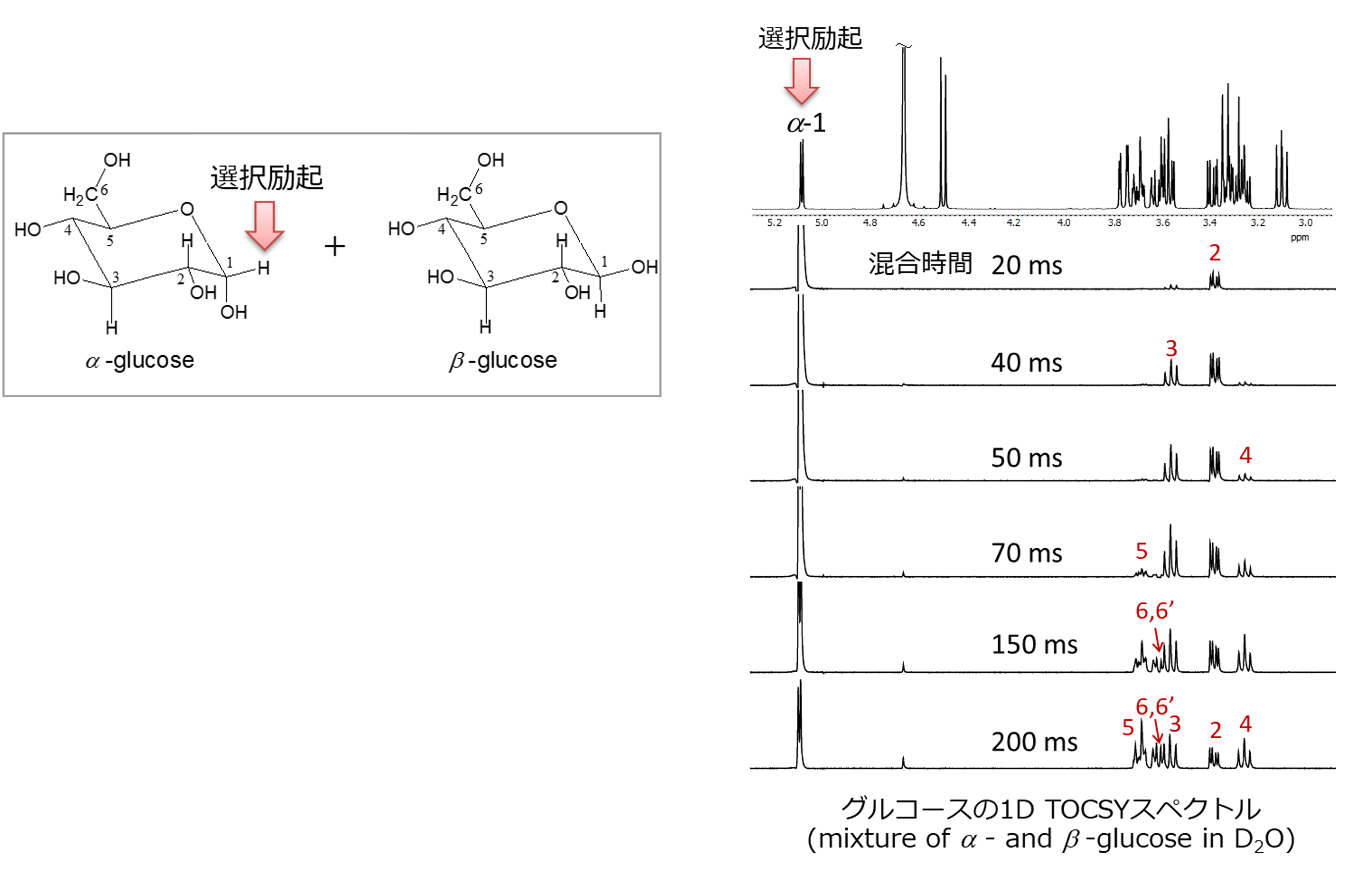
図14 グルコースの1D TOCSYスペクトル
混合時間を20 ms から200 ms まで変えていくと、α型グルコースの1位のアノメリック1Hをリレーの出発点としたスピンネットワークを追跡することができました。
混合時間:200msの1番下のスペクトルは、 αグルコースとβグルコースの混合スペクトルから、αグルコースのスピンネットワークだけを抽出したものになっています。
また、先ほど説明したように、1次元のTOCSYの方が、2次元のスライスデータより、デジタル分解能が良いこともわかります。
このように、混み合ったスペクトルから、スピン結合で繋がっている対象を抽出・確認するには、1D TOCSYのほうが有効です。
目的に応じて、 1D TOCSY 、2D TOCSY を使い分けることをお奨めします。
関連アプリケーション
二次元19F-19F TOCSYによる混合物の分離 -成分ごとに一次元19Fスペクトルを得る方法-
GEMSTONE-TOCSY (高選択性 1D TOCSY)
お問い合わせ
TOCSYやHSQC-TOCSYを用いたスピンネットワーク解析やNMR装置の詳細についてご興味がありましたら、ぜひ日本電子までお問い合わせください。豊富なアプリケーション事例と技術サポートにより、皆さまの分子構造解析を力強くバックアップいたします。
カタログダウンロード
製品情報

核磁気共鳴装置 (NMR)
NMRとは、Nuclear Magnetic Resonance (核磁気共鳴) の略で、原子核を磁場の中に入れて核スピンの共鳴現象を観測することで、物質の分子構造を原子レベルで解析するための装置です。特に、有機化合物および高分子材料の分析に威力を発揮し、製薬・バイオ・食品・化学といった分野で使われていますが、最近ではセラミックや電池などの無機材料の構造・物性解析にも適用範囲を広げています。

超伝導マグネット (SCM)
超伝導マグネット (SCM: Super Conducting Magnet) JJシリーズは新設計の超伝導線材とクライオスタットを備えた小型・ヘリウム低消費マグネットです。

日本電子株式会社
日本電子は、1949年の創業以来、これまで最先端の理科学・計測機器、産業機器そして医用機器の開発に邁進してきました。
今では数多くの製品が世界のいたるところで使用され、真のグローバル企業として高い評価を頂いております。
「世界の科学技術を支えるニッチトップ企業」を目指し、ますます高度化し多様化するお客様のニーズに的確にお応えしていきます。







